1. กำหนดให้
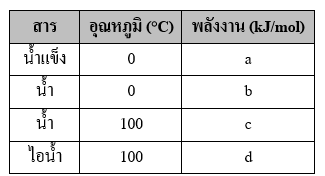
ถ้าน้ำแข็งที่ 0°C เปลี่ยนสถานะเป็นไอน้ำที่ 100°C ที่ความดัน 1 บรรยากาศ จะต้องใช้พลังงานกี่กิโลจูลต่อโมล |
| |
1. a+b+c+d |
2. d-c+b-a |
| |
3. c+d-a+d |
4. d-a |
| |
|
2. พิจารณาปรากฏการณ์ต่อไปนี้
1. การเกิดน้ำค้าง
2. การบูรระเหิดในตู้เสื้อผ้า
3. การระเบิดของดินปืน
4. ไอศกรีมละลายเมื่อวางทิ้งไว้
5. การสังเคราะห์แสงของพืช
6. โซเดียมไฮดรอกไซด์ละลายน้ำในบีกเกอร์แล้วบีกเกอร์ร้อนขึ้น
ข้อใดเป็นปรากฏการณ์ที่คายความร้อน |
| |
1. 1, 3 และ 6 |
2. 1, 4 และ 5 |
| |
3. 2, 3 และ 4 |
4. 2, 4 และ 5 |
| |
|
|
3. เมื่อนำชิ้นสังกะสีใส่ในสารละลายกรดไฮโดรคลอริก วิธีทำให้ปฏิกิริยาเกิดเร็วขึ้นโดยไม่เพิ่มปริมาณสังกะสีและกรดต่อไปนี้ข้อใดถูกต้อง
1. ใช้แท่งแก้วคนให้ทั่ว
2. ใช้ผงสังกะสีน้ำหนักเท่ากันแทนชิ้นสังกะสี
3. ให้ความร้อน
4. เติมน้ำกลั่นลงไปเท่าตัว |
| |
1. 1, 2, 3 เท่านั้น |
2. 2, 3, 4 เท่านั้น |
| |
3. 1, 3, 4 เท่านั้น |
4. 1, 2, 3,4 |
| |
|
|
| 4. มีปฏิกิริยาระหว่างของแข็งกับแก๊สชนิดหนึ่ง ซึ่งสามารถเกิดขึ้นได้ตลอดเวลา ถ้าต้องการทำให้อัตราการเกิดปฏิกิริยาเพิ่มขึ้นจะต้องทำให้มีการเปลี่ยนแปลงอะไร |
| |
1. ลดความดันของแก๊ส |
2. ลดอุณหภูมิลง |
| |
3. ลดขนาดของของแข็งลง |
4. รักษาความกดดันให้คงที่ |
| |
|
|
| 5. การทดลองในข้อใดมีอัตราการเกิดปฏิกิริยาสูงที่สุดที่อุณหภูมิเดียวกัน |
| |
1. ใส่แผ่นสังกะสี 1 ชิ้น หนัก 1 กรัม ลงในกรด HCl 10% โดยมวล/ปริมาตร |
| |
2. ใส่แผ่นสังกะสี 2 ชิ้น หนักชิ้นละ 0.5 กรัม ลงในกรด HCl 20% โดยมวล/ปริมาตร |
| |
3. ใส่สังกะสีผงละเอียด หนัก 1 กรัม ลงในกรด HCl 10% โดยมวล/ปริมาตร |
| |
4. ใส่สังกะสีผงละเอียด หนัก 1 กรัม ลงในกรด HCl 20% โดยมวล/ปริมาตร |
| |
|
|
| 6. ถ้าผสมสารละลาย HClกับสาร Cr2(CO3)3ผลิตภัณฑ์ชนิดหนึ่งที่ได้จากสมการที่ดุลแล้วคือข้อใด |
| |
1. 2CrCl2 |
2. Cr2O3 |
| |
3. 3CO2 |
4. 6H2O |
| |
|
|
| 7. ข้อใดเป็นระบบปิด |
| |
1. เติมแคลเซียมคลอไรด์ลงในสารละลายโซเดียมคาร์บอเนต |
| |
2. ผงสังกะสีใส่ในกรดไฮโดรคลอริก |
| |
3. เผาหินปูน |
| |
4. เติมกรดซัลฟิวริกลงในสารละลายโพแทสเซียมคาร์บอเนต |
| |
|
|
| 8. ปัจจัยที่มีอิทธิพลต่ออัตราการเกิดปฏิกิริยาเคมี คือข้อใด |
| |
1. ความเข้มข้นของสารละลาย ความดัน ตัวเร่ง พันธะโคเวเลนต์ |
| |
2. พันธะโคเวเลนต์ อุณหภูมิ ความเข้มข้นของสารละลาย ความดัน |
| |
3. อุณหภูมิ ความเข้มข้นของสารละลาย พื้นที่ผิว ตัวเร่ง |
| |
4. อุณหภูมิ พันธะโคเวเลนต์ พื้นที่ผิว ตัวเร่ง |
| |
|
|
| 9. ปฏิกิริยาระหว่างสาร A และสาร B ถ้าใส่สาร X ลงไป ปรากฏว่าอัตราการเกิดปฏิกิริยาเคมีจะช้าลง แต่ถ้าใส่สารY ลงไป ปรากฏว่าอัตราการเกิดปฏิกิริยาเคมีจะเร็วขึ้น สาร X และ Y คือ อะไร |
| |
1. X คือสารตั้งต้น Y คือผลิตภัณฑ์ |
2. X คือผลิตภัณฑ์ Y คือสารตั้งต้น |
| |
3. X คือตัวเร่งปฏิกิริยา Yคือตัวยับยั้งปฏิกิริยา |
4. X คือตัวยับยั้งปฏิกิริยา Yคือตัวเร่งปฏิกิริยา |
| |
|
|
| 10. เมื่อเผาแมกนีเซียม 1.5 กรัม จะรวมพอดีกับออกซิเจน 1.0 กรัม ถ้าต้องการเผาแมกนีเซียม 7.6 กรัมให้หมดพอดี จะต้องใช้ออกซิเจนกี่กรัม |
| |
1. 2.2 กรัม |
2. 2.8 กรัม |
| |
3. 5 กรัม |
4. 7.8 กรัม |
| |
|
|
11. การทดลองใดที่มวลของสารไม่เปลี่ยนแปลง
1. เผาเลด (II) ไนเตรท
2. เติมสารละลายโพแทสเซียมไอโอไดด์ลงในสารละลายเลด (II)ไนเตรท
3. เติมกรดลงในเบส |
| |
1. ข้อ 1 และ 2 |
2. ข้อ 1 และ 3 |
| |
3. ข้อ 2 และ 3 |
4. ข้อ 1 , 2 และ 3 |
| |
|
|
| 12. ปฏิกิริยาตามข้อใดที่ไม่เกิดแก๊ส |
| |
1. กรดไฮโดรคลอริกกับสังกะสี |
2. กรดแอซีติกกับโซเดียมไฮโดรเจนคาร์บอเนต |
| |
3. ปูนขาวกับแอมโมเนียมคลอไรด์ |
4. กรดซัลฟิวริกกับสารละลายแบเรียมคลอไรด์ |
| |
|
|
| 13. ฝนกรด เกิดจากข้อใด |
| |
1. ออกไซด์ของไนโตรเจนและซัลเฟอร์ละลายน้ำในอากาศ |
2. ออกไซด์ของคาร์บอนละลายน้ำในอากาศ |
| |
3. ไฮโดรเจนซัลไฟด์ละลายน้ำในอากาศ |
4. ไม่มีข้อใดถูก |
| |
|
|
| 14. ปฏิกิริยาระหว่างแคลเซียมไฮดรอกไซด์และแอมโมเนียมไนเตรตได้แก๊สชนิดหนึ่งเกิดขึ้น เมื่อทดสอบแก๊สด้วยกระดาษลิตมัสพบว่ากระดาษลิตมัสเปลี่ยนสีจากสีแดงเป็นสีน้ำเงิน แก๊สที่เกิดขึ้นคือแก๊สใด |
| |
1. NO3 |
2. NH3 |
| |
3. H2 |
4. N2O |
| |
|
|
| 15. การกระทำในข้อใดไม่มีผลต่ออัตราการเกิดปฏิกิริยาเคมี |
| |
1. การนำเนื้อหมูแช่ในช่องแช่แข็ง |
2. ใช้แคลเซียมคาร์ไบด์ช่วยในการบ่มมะม่วง |
| |
3. การเคี้ยวยาลดกรดชนิดเม็ดให้ละเอียดก่อนกลืน |
4. การเปลี่ยนขนาดภาชนะที่บรรจุสารละลายที่ทำปฏิกิริยา |
| |
|
|

